Peptidy jsou třídou sloučenin vytvořených spojením více aminokyselin prostřednictvím peptidových vazeb.Jsou všudypřítomné v živých organismech.Doposud byly v živých organismech nalezeny desítky tisíc peptidů.Peptidy hrají důležitou roli při regulaci funkčních aktivit různých systémů, orgánů, tkání a buněk a v životních aktivitách a často se používají ve funkční analýze, výzkumu protilátek, vývoji léků a dalších oblastech.S rozvojem biotechnologie a technologie syntézy peptidů bylo vyvinuto a aplikováno stále více peptidových léků v klinice.
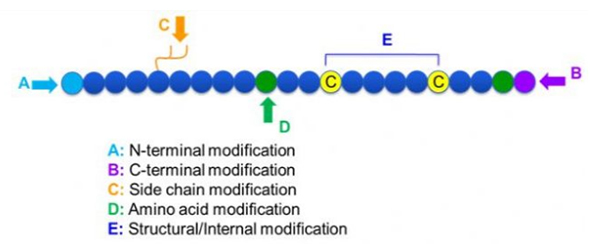
Existuje široká škála modifikací peptidů, které lze jednoduše rozdělit na postmodifikaci a procesní modifikaci (s použitím odvozené modifikace aminokyselin), a N-koncovou modifikaci, C-koncovou modifikaci, modifikaci postranního řetězce, modifikaci aminokyselin, modifikaci skeletu, atd., v závislosti na místě úpravy (obrázek 1).Jako důležitý prostředek ke změně struktury hlavního řetězce nebo skupin postranních řetězců peptidových řetězců může modifikace peptidů účinně změnit fyzikální a chemické vlastnosti peptidových sloučenin, zvýšit rozpustnost ve vodě, prodloužit dobu působení in vivo, změnit jejich biologickou distribuci, odstranit imunogenicitu. , snížit toxické vedlejší účinky atd. V tomto článku je představeno několik hlavních strategií modifikace peptidů a jejich charakteristiky.
1. Cyklizace
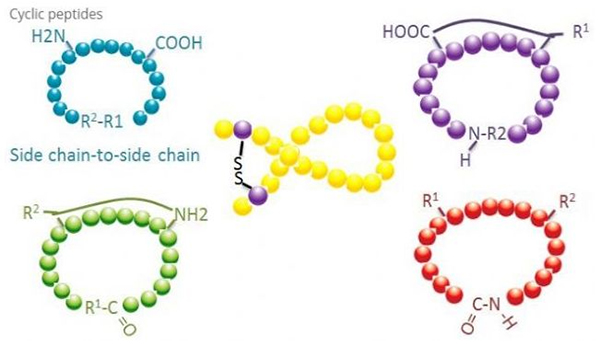
Cyklické peptidy mají mnoho aplikací v biomedicíně a mnoho přírodních peptidů s biologickou aktivitou jsou cyklické peptidy.Protože cyklické peptidy mají tendenci být rigidnější než lineární peptidy, jsou extrémně odolné vůči trávicímu systému, mohou přežívat v trávicím traktu a vykazují silnější afinitu k cílovým receptorům.Cyklizace je nejpřímější způsob syntézy cyklických peptidů, zejména pro peptidy s velkou strukturní kostrou.Podle režimu cyklizace jej lze rozdělit na typ s postranním řetězcem, koncový - typ postranního řetězce, koncový - koncový typ (typ end to end).
(1) sidechain-to-sidechain
Nejběžnějším typem cyklizace postranního řetězce na postranní řetězec je disulfidové přemostění mezi cysteinovými zbytky.Tato cyklizace je zavedena párem cysteinových zbytků, které jsou zbaveny ochrany a poté oxidovány za vzniku disulfidových vazeb.Polycyklické syntézy lze dosáhnout selektivním odstraněním sulfhydrylových ochranných skupin.Cyklizaci lze provést buď v post-disociačním rozpouštědle nebo na pre-disociační pryskyřici.Cyklizace na pryskyřicích může být méně účinná než cyklizace v rozpouštědle, protože peptidy na pryskyřicích netvoří snadno cyklizované konformace.Dalším typem cyklizace postranního řetězce - postranního řetězce je tvorba amidové struktury mezi zbytkem kyseliny asparagové nebo kyseliny glutamové a bazickou aminokyselinou, což vyžaduje, aby skupina chránící postranní řetězec musela být schopna selektivně odstranit z polypeptidu buď na pryskyřici nebo po disociaci.Třetím typem postranního řetězce - cyklizace postranního řetězce je tvorba difenyletherů tyrosinem nebo p-hydroxyfenylglycinem.Tento typ cyklizace v přírodních produktech se vyskytuje pouze v mikrobiálních produktech a produkty cyklizace mají často potenciální léčivou hodnotu.Příprava těchto sloučenin vyžaduje jedinečné reakční podmínky, takže se při syntéze konvenčních peptidů často nepoužívají.
(2) terminál-to-sidechain
Cyklizace koncového postranního řetězce obvykle zahrnuje C-konec s aminoskupinou lysinového nebo ornithinového postranního řetězce nebo N-koncový postranní řetězec kyseliny asparagové nebo kyseliny glutamové.Jiná cyklizace polypeptidu se provádí vytvořením etherových vazeb mezi koncovým C a serinovým nebo threoninovým postranním řetězcem.
(3) Typ koncového nebo typu hlava-ocas
Polypeptidy řetězce mohou být buď cyklovány v rozpouštědle, nebo fixovány na pryskyřici cyklací postranního řetězce.Nízké koncentrace peptidů by měly být použity při centralizaci rozpouštědel, aby se zabránilo oligomerizaci peptidů.Výtěžek syntetického kruhového polypeptidu typu head-to-tail závisí na sekvenci polypeptidového řetězce.Proto před přípravou cyklických peptidů ve velkém měřítku by měla být nejprve vytvořena knihovna možných řetězených vedoucích peptidů, následovaná cyklizací, aby se našla sekvence s nejlepšími výsledky.
2. N-methylace
N-methylace se původně vyskytuje v přírodních peptidech a je zavedena do syntézy peptidů, aby se zabránilo tvorbě vodíkových vazeb, čímž jsou peptidy odolnější vůči biologickému rozkladu a clearance.Nejdůležitější metodou je syntéza peptidů za použití derivátů N-methylovaných aminokyselin.Kromě toho může být také použita Mitsunobuova reakce meziproduktů N-(2-nitrobenzensulfonylchlorid) polypeptid-pryskyřice s methanolem.Tato metoda byla použita pro přípravu cyklických peptidových knihoven obsahujících N-methylované aminokyseliny.
3. Fosforylace
Fosforylace je jednou z nejběžnějších posttranslačních modifikací v přírodě.V lidských buňkách je fosforylováno více než 30 % proteinů.Fosforylace, zejména reverzibilní fosforylace, hraje důležitou roli při řízení mnoha buněčných procesů, jako je signální transdukce, genová exprese, regulace buněčného cyklu a cytoskeletu a apoptóza.
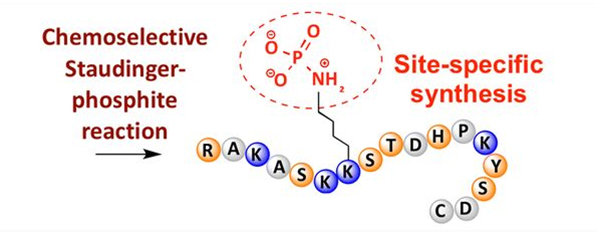
Fosforylaci lze pozorovat na různých aminokyselinových zbytcích, ale nejběžnějšími cíli fosforylace jsou serinové, threoninové a tyrosinové zbytky.Fosfotyrosinové, fosfothreoninové a fosfoserinové deriváty mohou být buď zavedeny do peptidů během syntézy nebo vytvořeny po syntéze peptidů.Selektivní fosforylace může být dosaženo použitím zbytků serinu, threoninu a tyrosinu, které selektivně odstraňují chránící skupiny.Některá fosforylační činidla mohou také zavést skupiny kyseliny fosforečné do polypeptidu dodatečnou modifikací.V posledních letech bylo dosaženo místně specifické fosforylace lysinu pomocí chemicky selektivní Staudinger-fosfitové reakce (obrázek 3).
4. Myristoylace a palmitoylace
Acylace N-konce mastnými kyselinami umožňuje peptidům nebo proteinům vázat se na buněčné membrány.Myridamoylovaná sekvence na N-konci umožňuje, aby proteinkinázy rodiny Src a proteiny Gaq s reverzní transkriptázou byly zaměřeny na vazbu na buněčné membrány.Kyselina myristová byla navázána na N-konec pryskyřice-polypeptid pomocí standardních kopulačních reakcí a výsledný lipopeptid mohl být disociován za standardních podmínek a čištěn pomocí RP-HPLC.
5. Glykosylace
Glykopeptidy jako vankomycin a teicolanin jsou důležitá antibiotika pro léčbu bakteriálních infekcí rezistentních vůči lékům a další glykopeptidy se často používají ke stimulaci imunitního systému.Navíc, protože mnoho mikrobiálních antigenů je glykosylováno, je velmi důležité studovat glykopeptidy pro zlepšení terapeutického účinku infekce.Na druhé straně bylo zjištěno, že proteiny na buněčné membráně nádorových buněk vykazují abnormální glykosylaci, díky které hrají glykopeptidy důležitou roli ve výzkumu rakoviny a imunitní obrany nádorů.Glykopeptidy se připravují metodou Fmoc/t-Bu.Glykosylované zbytky, jako je threonin a serin, jsou často zaváděny do polypeptidů pomocí fMOC aktivovaných esterem pentafluorfenolu, aby se chránily glykosylované aminokyseliny.
6. Isopren
Isopentadienylace se vyskytuje na cysteinových zbytcích v postranním řetězci blízko C-konce.Proteinový isopren může zlepšit afinitu buněčné membrány a vytvořit interakci protein-protein.Mezi izopentadienované proteiny patří tyrosin fosfatáza, malá GTáza, molekuly cochaperonu, jaderná lamina a centromerické vazebné proteiny.Isoprenové polypeptidy mohou být připraveny použitím isoprenu na pryskyřicích nebo zavedením cysteinových derivátů.
7. Modifikace polyethylenglykolu (PEG).
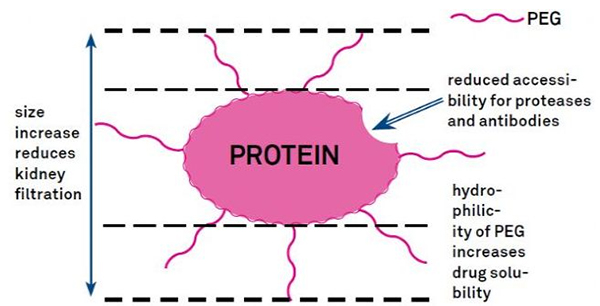
Modifikace PEG lze použít ke zlepšení hydrolytické stability proteinu, biologické distribuce a rozpustnosti peptidu.Zavedení PEG řetězců do peptidů může zlepšit jejich farmakologické vlastnosti a také inhibovat hydrolýzu peptidů proteolytickými enzymy.PEG peptidy procházejí glomerulárním kapilárním průřezem snadněji než běžné peptidy, což výrazně snižuje renální clearance.Vzhledem k prodlouženému aktivnímu poločasu PEG peptidů in vivo může být normální úroveň léčby udržována nižšími dávkami a méně častými peptidovými léky.Modifikace PEG má však také negativní účinky.Velká množství PEG brání enzymu v degradaci peptidu a také snižují vazbu peptidu na cílový receptor.Nízká afinita PEG peptidů je však obvykle kompenzována jejich delším farmakokinetickým poločasem a tím, že jsou PEG peptidy přítomny v těle déle, mají větší pravděpodobnost, že budou absorbovány do cílových tkání.Specifikace PEG polymeru by proto měly být optimalizovány pro optimální výsledky.Na druhé straně se PEG peptidy hromadí v játrech v důsledku snížené renální clearance, což vede k makromolekulárnímu syndromu.Proto musí být modifikace PEG navrženy pečlivěji, když se peptidy používají pro testování léčiv.
Běžné modifikační skupiny PEG modifikátorů lze zhruba shrnout takto: Amino (-amin) -NH2, aminomethyl-Ch2-NH2, hydroxy-OH, karboxy-Cooh, sulfhydryl (-Thiol) -SH, maleimid -MAL, sukcinimid karbonát - SC, sukcinimidacetát -SCM, sukcinimid propionát -SPA, n-hydroxysukcinimid -NHS, Acrylate-ch2ch2cooh, aldehyd -CHO (jako propional-ald, butyrALD), akrylová báze (-akrylát-acrl), azido-azid, biotinyl - Biotin, fluorescein, glutaryl-GA, akryláthydrazid, alkyne-alkin, p-toluensulfonát -OTs, sukcinimid sukcinát -SS, atd. PEG deriváty s karboxylovými kyselinami mohou být navázány na n-koncové aminy nebo lysinové postranní řetězce.Amino-aktivovaný PEG může být navázán na postranní řetězce kyseliny asparagové nebo kyseliny glutamové.Mal-aktivovaný PEG může být konjugován s merkaptanem z plně deprotektovaných cysteinových postranních řetězců [11].Modifikátory PEG jsou běžně klasifikovány následovně (poznámka: mPEG je methoxy-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) modifikátor PEG s přímým řetězcem
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) bifunkční modifikátor PEG
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) větvený PEG modifikátor
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotinizace
Biotin může být silně vázán s avidinem nebo streptavidinem a vazebná síla je dokonce blízká kovalentní vazbě.Biotinem značené peptidy se běžně používají v imunotestech, histocytochemii a průtokové cytometrii založené na fluorescenci.K navázání biotinylovaných peptidů lze také použít značené antibiotinové protilátky.Biotinové značky jsou často připojeny k postrannímu řetězci lysinu nebo N-konci.Kyselina 6-aminokapronová se často používá jako vazba mezi peptidy a biotinem.Vazba je flexibilní ve vazbě na substrát a lépe se váže v přítomnosti sterické zábrany.
9. Fluorescenční značení
Fluorescenční značení lze použít ke sledování polypeptidů v živých buňkách a ke studiu enzymů a mechanismů účinku.Tryptofan (Trp) je fluorescenční, takže jej lze použít pro vnitřní značení.Emisní spektrum tryptofanu závisí na periferním prostředí a snižuje se s klesající polaritou rozpouštědla, což je vlastnost, která je užitečná pro detekci peptidové struktury a vazby na receptor.Fluorescence tryptofanu může být zhášena protonovanou kyselinou asparagovou a kyselinou glutamovou, což může omezit její použití.Dansylchloridová skupina (Dansyl) je vysoce fluorescenční, když je navázána na aminoskupinu a často se používá jako fluorescenční značka pro aminokyseliny nebo proteiny.
Fluorescenční rezonance Přeměna energie (FRET) je užitečná pro enzymové studie.Když je aplikován FRET, substrátový polypeptid obvykle obsahuje fluorescenčně značící skupinu a fluorescenční zhášecí skupinu.Značené fluorescenční skupiny jsou zhášeny zhášečem prostřednictvím nefotonového přenosu energie.Když je peptid disociován od příslušného enzymu, značící skupina emituje fluorescenci.
10. Polypeptidy v kleci
Peptidy v kleci mají opticky odstranitelné ochranné skupiny, které chrání peptid před navázáním na receptor.Při vystavení UV záření se peptid aktivuje, čímž se obnoví jeho afinita k receptoru.Protože tato optická aktivace může být řízena podle času, amplitudy nebo umístění, mohou být peptidy v kleci použity ke studiu reakcí probíhajících v buňkách.Nejčastěji používanými ochrannými skupinami pro polypeptidy v kleci jsou 2-nitrobenzylové skupiny a jejich deriváty, které mohou být zavedeny do syntézy peptidů prostřednictvím ochranných derivátů aminokyselin.Deriváty aminokyselin, které byly vyvinuty, jsou lysin, cystein, serin a tyrosin.Deriváty aspartátu a glutamátu se však běžně nepoužívají kvůli jejich náchylnosti k cyklizaci během syntézy a disociace peptidů.
11. Polyantigenní peptid (MAP)
Krátké peptidy obvykle nejsou imunní a musí být spojeny s nosnými proteiny, aby se vytvořily protilátky.Polyantigenní peptid (MAP) je složen z více identických peptidů spojených s lysinovými jádry, které mohou specificky exprimovat vysoce účinné imunogeny a lze je použít k přípravě párů peptid-nosič protein.Polypeptidy MAP lze syntetizovat syntézou na pevné fázi na pryskyřici MAP.Neúplná vazba však vede k chybějícím nebo zkráceným peptidovým řetězcům na některých větvích, a proto nevykazuje vlastnosti původního MAP polypeptidu.Alternativně mohou být peptidy připraveny a purifikovány odděleně a poté navázány na MAP.Peptidová sekvence připojená k peptidovému jádru je dobře definovaná a snadno charakterizována hmotnostní spektrometrií.
Závěr
Modifikace peptidů je důležitým prostředkem pro navrhování peptidů.Chemicky modifikované peptidy mohou nejen udržet vysokou biologickou aktivitu, ale také účinně zabránit nevýhodám imunogenicity a toxicity.Chemická modifikace může zároveň poskytnout peptidům některé nové vynikající vlastnosti.V posledních letech se rychle rozvinula metoda aktivace CH pro post-modifikace polypeptidů a bylo dosaženo mnoha důležitých výsledků.
Čas odeslání: 20. března 2023
